
Донорно-акцепторная связь, координационная связь, термин, обозначающий один из способов образования химической ковалентной связи. Обычная ковалентная связь между двумя атомами обусловлена взаимодействием двух электронов — по одному от каждого атома. Д.-а. с. осуществляется за счёт пары электронов одного атома (донора) и свободной (незаполненной) орбитали другого (акцептора). Схематически это различие можно выразить так:

В обоих случаях электроны становятся общими для двух атомов. Типичным примером является образование иона аммония при реакции аммиака с ионом водорода (протоном):
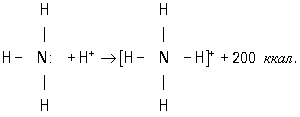
В молекуле аммиака азот имеет неподелённую пару электронов, у иона водорода 1s-орбиталь свободна. При достаточном сближении молекулы NH3 и иона Н+ двухэлектронное облако азота попадает в сферу притяжения иона водорода и становится общим и для атома азота, и для атома водорода, т. е. возникает четвёртая ковалентная связь N — Н. Все связи N — Н в этом ионе становятся равноценными и неразличимыми. Ещё один важный пример — образование иона оксония:

В данном случае молекула воды — донор, протон — акцептор.
Этот способ образования ковалентной связи играет большую роль в химии комплексных соединений.