
Мезомерия (от мезо... и греч. méros — часть), сопряжение, резонанс в сопряжённых системах, характер распределения электронной плотности в молекулах, который можно трактовать как частичную делокализацию связей и зарядов атомов. Так, в карбоксилат-анионе, согласно классической структуре, один из атомов кислорода связан с атомом углерода простой связью и несёт полный отрицательный заряд, другой соединён двойной связью и нейтрален. Такая структура может быть выражена двумя равноценными формулами I и II (см. ниже). Опыт же показывает, что оба атома кислорода равноценны, т. е. каждый из них несёт один и тот же частичный отрицательный заряд, а обе связи с атомом С имеют одинаковую длину. Т. о., истинная структура является промежуточной между I и II; она может быть изображена как резонансный гибрид канонических (крайних) структур I и II (см. Резонанса теория) или мезомерной формулой III, в которой изогнутые стрелки показывают направление смещения электронов, приводящего к выравниванию зарядов и связей:

М. ярко проявляется в сопряжённых системах (см. Сопряжение связей). Обычно она выражает состояние, промежуточное между классической структурой и структурой (или структурами) с полностью разделёнными зарядами, например:
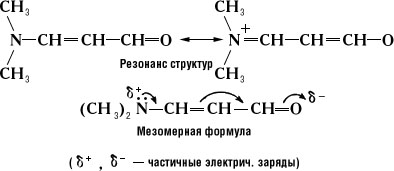
В циклически сопряжённых системах мезомерное смещение не всегда приводит к разделению зарядов. Так, строение бензола может быть представлено как резонансный гибрид двух классических структур Кекуле (IV и V) или же мезомерной формулой VI, отражающей равноценность всех шести атомов углерода и всех связей между ними:

Мезомерный эффект с небольшим ослабеванием передаётся по системе сопряжённых связей (поэтому он называется также эффектом сопряжения). Группы, несущие неподелённую электронную пару ( , RÖ–, HÖ–, галогены), обладают положительным мезомерным эффектом (+М-эффект) и могут увеличивать электронную плотность остальной части системы; группы
, RÖ–, HÖ–, галогены), обладают положительным мезомерным эффектом (+М-эффект) и могут увеличивать электронную плотность остальной части системы; группы  ,
,  ,
, 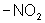 и т.п. уменьшают электронную плотность (— М-эффект):
и т.п. уменьшают электронную плотность (— М-эффект):
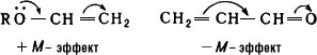
Представление о М. позволяет объяснить многие свойства веществ и механизмы реакций в органической химии. Количественная картина распределения электронной плотности в молекулах может быть получена путём квантовомеханических расчётов (см. Квантовая химия).
Концепция М. разработана главным образом английским химиком К. Инголдом в 1926.
Лит.: Несмеянов А. Н., Несмеянов Н. А., Начала органической химии, кн. 1, М., 1969.
Б. Л. Дяткин.