
Перекисные соединения, класс химических соединений, содержащих непосредственно связанные между собой атомы кислорода.
Перекисные соединения неорганические. Простейший, наиболее важный и распространённый представитель этой группы — перекись водорода H2O2. Кристаллические решётки неорганических П. с. состоят из ионов металлов и из молекулярных анионов кислорода O22-, O2- и O3-. Соответственно по наличию этих групп различают перекиси, надперекиси и озониды. Все они являются различной силы окислителями, а при слабых термических или химических воздействиях разлагаются с выделением кислорода. Наиболее просто — сжиганием на воздухе или в кислороде — получают перекиси и надперекиси щелочных металлов: Na2O2, K2O2 (перекиси), KO2, RbO2, CsO2 (надперекиси). Перекиси и надперекиси металлов — соли слабых кислот, соответственно перекиси водорода H2O2 и пергидроксила HO2. Сам пергидроксил — активная частица и при обычных температурах быстро превращается в H2O2 и O2.
Пергидроксил — промежуточная частица большинства химических процессов горения и окисления кислородом и перекисью водорода. Действием озона (O3) на гидроокиси или надперекиси получают озониды щелочных металлов MO3 (например, KO3). Термическая нестойкость, окислительная активность, количество способного выделиться кислорода растут в ряду перекиси — надперекиси — озониды. Гидролиз этих П. с. происходит с образованием различных по силе окислителей (насыщенных соединений, как H2O2, или частиц, как OH):
M2O2 + 2H2O = 2MOH + H2O2,
M2O2 + H2O = MOH + HO2,
MO3 + H2O = MOH + HO + O2.
К этим группам соединений примыкают пероксигидраты — соединения, содержащие вместо кристаллизационной воды кристаллизационную H2O2, например K2CO3.3H2O2, в том числе и пероксигидраты перекисей, например CaO2.2H2O2.
Пероксогруппа — O — O — входит в состав пероксо- или надкислот и двуядерных комплексных соединений. Примером служат пероксосерные кислоты — пероксомоно- и пероксодисерная,
HOSO2 — ООН
и
HOSO2 — O — O — SO2OH.
Аналогичные пероксопроизводные известны для угольной и некоторых других кислот. Эти соединения получают либо путём электролиза обычных кислот, либо при взаимодействии концентрированных кислот и H2O2. Двуядерные комплексы, содержащие пероксогруппу, известны для ряда металлов, а наиболее изучены для комплексов кобальта; многие из них могут быть получены при взаимодействии кислорода с солями кобальта (в растворе или в кристаллическом состоянии). Большинство пероксосоединений водой гидролизуется с образованием H2O2.
П. с. нашли применение в технике как окислители (пероксодисерная кислота, перекись натрия), отбеливатели (пероксобораты, например NaBO3; пероксокар-бонаты, например Na2CO3), как удобные источники кислорода для регенерации воздуха — эквивалентного превращения CO2 в O2 (надперекиси NaO2, KO2). Некоторые комплексные пероксосоли обратимо присоединяют, а при нагревании или изменении кислотности раствора выделяют кислород. На этом основано их применение как «кислородных батарей», как переносчиков кислорода, для разделения азотно-кислородных смесей. Различие в строении неорганических П. с. обусловливает различие их физических свойств и реакционной способности и возможность применения в разнообразных условиях.
А. П. Пурмаль.
Перекисные соединения органические содержат группировку — О — О —, связанную с одним или двумя атомами углерода. Основные типы органических П. с.: 1) перекиси алкилов и арилов R — O — O — R (здесь и далее R — алкил или арил); 2) перекиси ацилов RCO—O—O—COR; 3) гидроперекиси R — O — O — Н; 4) перкислоты (надкислоты) RCO — O — O — H. К ним примыкают соединения, в которых перекисная группировка связана с гетероатомом, например R3Si — O — O — Li, R2B — O — OR, и озониды, содержащие группировки — О — О — О —, например CF3 — O — O — O — CF3.
П. с. получают главным образом окислением различных органических соединений (например, насыщенных углеводородов, олефинов, спиртов, альдегидов, кетонов, металлоорганических соединений) кислородом (часто — фотохимически) или перекисью водорода, например:

Перекиси ацилов и надкислоты получаются взаимодействием карбоновых кислот или их производных с перекисью водорода в присутствии оснований:
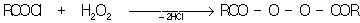

Перекись диметила CH3OOCH3 — газ, tкип — 13 °С; перекись ди-трет-бутила — tкип 70 °С (при 197 мм рт. ст.); перекись ацетила (CH3COO)2 — tпл 27 °С, tкип 63 °С (при 21 мм рт. ст.), перекись бензоила (C6H5COO)2 — tпл 106—108 °С; надбензойная кислота C6H5CO — O — O — H — tпл 41—43 °C. Известны полимерные П. с. типа
.
При нагревании или облучении ультрафиолетовым светом органических П. с. происходит разрыв кислород-кислородной связи с образованием свободных радикалов типа RO× или RCO — O×, дальнейшая судьба которых (а следовательно, и общее направление реакции) зависит от характера R. Алкоксильные или ацилоксильные радикалы чаще всего распадаются дальше, давая свободные углеводородные радикалы, например:
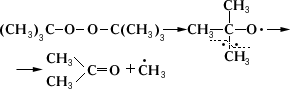
Образующиеся свободные радикалы могут вызвать цепной распад П. с., поэтому многие из них, особенно низшие, взрывчаты. Это необходимо учитывать при работе с олефинами, диенами и простыми эфирами, легко образующими П. с. при действии кислорода воздуха. Стабильность П. с. возрастает с увеличением электроотрицательности заместителей, связанных с перекисной группой, а также при переходе от первичных радикалов к вторичным и третичным.
Органические П. с. (перекиси бензоила, ацетила, ди-трет-бутила) широко используют для инициирования свободнорадикальной полимеризации, вулканизации каучуков, а также таких реакций, как окисление, галогенирование, присоединение по двойным связям, теломеризация и др. П. с., особенно надкислоты, применяются в органическом синтезе как окислители, например для получения окисей олефинов (Прилежаева реакция), в текстильной промышленности — как отбеливающие вещества. П. с.— промежуточные продукты многих промышленно важных реакций, например синтеза фенола и ацетона окислением кумола; они играют большую роль в процессах горения и окислительных биохимических процессах.
Б. Л. Дяткин.
Лит.: Вольнов И. И., Перекиси, надперекиси и озониды щелочных и щелочною земельных металлов, М., 1964; его же, Современные воззрения на природу неорганических перекисных соединений, «Успехи химии», 1972, т. 41, в. 4; Карножицкий В., Органические перекиси, пер. с франц., М., 1961.