Ароматические соединения — различия между версиями
EvgBot (обсуждение | вклад) м (Новая: '''Ароматические соединения''', класс органических, или углеродистых, соединений. Наряду с классом жирн...) |
EvgBot (обсуждение | вклад) (заливка из БСЭ) |
||
| Строка 11: | Строка 11: | ||
[[Категория:Химические соединения]] | [[Категория:Химические соединения]] | ||
{{МСЭ}} | {{МСЭ}} | ||
| + | '''Ароматические соединения '''(от греч. árômа — благовоние), класс органических циклических соединений, все атомы которых участвуют в образовании единой сопряжённой системы; p-электроны такой системы образуют устойчивую, т. е. замкнутую, электронную оболочку. Название «А. с.» закрепилось вследствие того, что первые открытые и изученные представители этого класса веществ обладали приятным запахом. Простейшее А. с. — [[Бензол|бензол]] (1). К А. с. относятся также [[Нафталин|нафталин]] (II), [[Антрацен|антрацен]] (III), [[Фенантрен|фенантрен]] (IV) и др. соединения, содержащие конденсированные бензольные кольца, а также различные их производные. | ||
| + | |||
| + | [[Изображение:Ароматические соединения_i0_(БСЭ).gif]] | ||
| + | |||
| + | Выделение А. с. в особый класс органических соединений обусловлено рядом соображений. Бензол C<sub>6</sub>H<sub>6</sub>, содержащий формально 3 двойные связи, должен обладать свойствами сильно ненасыщенного соединения; между тем бензол и др. А. с. не изменяются при действии перманганата калия на холоду, не присоединяют тотчас же бром, как это наблюдается в случае олефинов, содержащих двойные связи. Для А. с. характерна лёгкость замещения атомов водорода, связанных с атомами углерода в бензольном кольце, при действии различных электрофильных реагентов (см. [[Нуклеофильные и электрофильные реагенты|Нуклеофильные и электрофильные реагенты]]). Так, при действии азотной кислоты на бензол образуется нитробензол: C<sub>6</sub>H<sub>6</sub> + HNO<sub>3</sub> ® C<sub>6</sub>H<sub>5</sub>NO<sub>2</sub> + H<sub>2</sub>O. | ||
| + | |||
| + | Аналогичные процессы электрофильного замещения происходят и при сульфировании, галогенировании, ацетилировании А. с., которые при этом ведут себя скорее как насыщенные, чем как ненасыщенные соединения. Следует, однако, иметь в виду, что лёгкость реакций замещения и затруднённость реакций присоединения к А. с. носят лишь количественный характер; в определённых условиях бензол присоединяет три молекулы хлора с образованием гексахлорциклогексана C<sub>6</sub>H<sub>6</sub>Cl<sub>6</sub>; гидрирование нафталина ведёт к присоединению пяти молекул водорода с образованием декалина. | ||
| + | |||
| + | А. с. очень устойчивы; образуются из других классов соединений в жёстких условиях. Так, бензол можно получить из ацетилена при 650°C в присутствии активного угля; бензол образуется также при дегидрировании («ароматизации») циклогексана (V). | ||
| + | |||
| + | Заместители в А. с. приобретают особые свойства. Например, фенолы обладают более кислыми свойствами, чем спирты, а нитрофенолы в этом отношении приближаются к карбоновым кислотам. Ароматические амины значительно более слабые основания, чем алифатические; для ароматических аминов, например анилина | ||
| + | |||
| + | [[Изображение:Ароматические соединения_i1_(БСЭ).gif]] | ||
| + | |||
| + | C<sub>6</sub>H<sub>5</sub>NH<sub>2</sub>, характерна реакция с азотистой кислотой — диазотирование, приводящая к [[Диазосоединения|диазосоединениям]], широко применяемым в производстве красителей. А. с. чрезвычайно многочисленны и имеют большое практическое значение. Так, ароматич. нитросоединения, сульфокислоты, фенолы, амины являются полупродуктами синтеза многих красителей, лекарственных веществ; фенолы, стирол, терефталевую кислоту используют для синтеза полимеров; из толуола получают взрывчатое вещество тротил и т.д. | ||
| + | |||
| + | Характерные особенности этого класса соединений могут быть объяснены тем, что А. с. на самом деле не содержат чередующихся простых и кратных связей; все связи в бензоле равноценны и совершенно выравнены; расстояния между атомами углерода в бензоле [[Изображение:Ароматические соединения_i2_(БСЭ).gif]] промежуточны между значениями межатомных расстояний в случае простой [[Изображение:Ароматические соединения_i3_(БСЭ).gif]] двойной [[Изображение:Ароматические соединения_i4_(БСЭ).gif]] связей. Поэтому строение бензола теперь предпочитают изображать не обычной формулой (1), а формулой (1а). Для бензола и др. А. с. характерно, что все p-электроны образуют устойчивую «замкнутую» электронную оболочку. | ||
| + | |||
| + | Позже было найдено, что сходными с А. с. свойствами обладают и многие другие «небензоидные» соединения. В первую очередь следует назвать ненасыщенные пятичленные [[Гетероциклические соединения|гетероциклические соединения]] типа [[Фуран|фурана]],'' [[Тиофен|тиофена]]'','' [[Пиррол|пиррола]]''. Ароматическими свойствами обладают и шестичленные гетероциклические соединения типа [[Пиридин|пиридина]]. | ||
| + | |||
| + | Известны небензоидные А. с., скелет которых состоит только из атомов углерода; к их числу относятся такие стабильные органические ионы, как катион тропилия (VI), анион циклопентадиенила (VII), биполярные соединения типа азуленов | ||
| + | |||
| + | [[Изображение:Ароматические соединения_i5_(БСЭ).gif]] | ||
| + | |||
| + | (VIII) и др. Ароматическими свойствами обладают и некоторые неорганические соединения, например [[Боразол|боразол]] (IX), фосфонитрилхлорид (X). Ароматичность бензоидных и небензоидных соединений, проявляющаяся в способности вступать в реакции электрофильного замещения, соответствует ряду: анион VII > пиррол > [[Бензол|бензол]] ® пиридин > тропилий; способность к реакциям нуклеофильного замещения изменяется в обратном порядке. | ||
| + | |||
| + | | ||
| + | |||
| + | ''Лит.:'' Карер П., Курс органической химии, пер. с нем., Л., 1960. | ||
| + | |||
| + | '' Я. Ф. Комиссаров.'' | ||
| + | {{БСЭ}} | ||
| + | |||
| + | |||
| + | |||
| + | [[Категория:Химия]] | ||
Версия 15:04, 30 января 2009
Ароматические соединения, класс органических, или углеродистых, соединений. Наряду с классом жирных соединений, является одним из крупнейших классов органической химии.
Главным источником А. с. является каменноугольная смола — продукт сухой перегонки каменного угля. Типичными представителями А. с. являются: бензол, фенол, анилин, нафталин. Количество А. с. исчисляется десятками тысяч. А. с. имеют громадное значение в промышленности. Анилиновые, нафталиновые и ализариновые краски; салициловые препараты, сахарин и целый ряд других фармацевтических препаратов и питательных веществ, пикриновая кислота, тринитротолуол (тротил) и другие взрывчатые вещества; пирогаллол, гидрохинон и друг. проявители, фенолфталеин и метилоранж и др. индикаторы и пр. имеют огромное значение в промышленности и технике. Название А. с. сохранилось только как историческое; оно было установлено в то время, когда производные бензола были известны как составные части бальзамов и благовонных масел. Химическая теория А. с. берет свое начало с работ Кекуле.
См. также
- В статье воспроизведен текст из Малой советской энциклопедии.
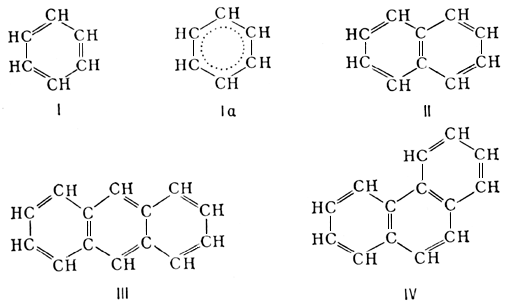
Ароматические соединения (от греч. árômа — благовоние), класс органических циклических соединений, все атомы которых участвуют в образовании единой сопряжённой системы; p-электроны такой системы образуют устойчивую, т. е. замкнутую, электронную оболочку. Название «А. с.» закрепилось вследствие того, что первые открытые и изученные представители этого класса веществ обладали приятным запахом. Простейшее А. с. — бензол (1). К А. с. относятся также нафталин (II), антрацен (III), фенантрен (IV) и др. соединения, содержащие конденсированные бензольные кольца, а также различные их производные.
Выделение А. с. в особый класс органических соединений обусловлено рядом соображений. Бензол C6H6, содержащий формально 3 двойные связи, должен обладать свойствами сильно ненасыщенного соединения; между тем бензол и др. А. с. не изменяются при действии перманганата калия на холоду, не присоединяют тотчас же бром, как это наблюдается в случае олефинов, содержащих двойные связи. Для А. с. характерна лёгкость замещения атомов водорода, связанных с атомами углерода в бензольном кольце, при действии различных электрофильных реагентов (см. Нуклеофильные и электрофильные реагенты). Так, при действии азотной кислоты на бензол образуется нитробензол: C6H6 + HNO3 ® C6H5NO2 + H2O.
Аналогичные процессы электрофильного замещения происходят и при сульфировании, галогенировании, ацетилировании А. с., которые при этом ведут себя скорее как насыщенные, чем как ненасыщенные соединения. Следует, однако, иметь в виду, что лёгкость реакций замещения и затруднённость реакций присоединения к А. с. носят лишь количественный характер; в определённых условиях бензол присоединяет три молекулы хлора с образованием гексахлорциклогексана C6H6Cl6; гидрирование нафталина ведёт к присоединению пяти молекул водорода с образованием декалина.
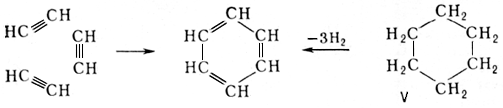
А. с. очень устойчивы; образуются из других классов соединений в жёстких условиях. Так, бензол можно получить из ацетилена при 650°C в присутствии активного угля; бензол образуется также при дегидрировании («ароматизации») циклогексана (V).
Заместители в А. с. приобретают особые свойства. Например, фенолы обладают более кислыми свойствами, чем спирты, а нитрофенолы в этом отношении приближаются к карбоновым кислотам. Ароматические амины значительно более слабые основания, чем алифатические; для ароматических аминов, например анилина
C6H5NH2, характерна реакция с азотистой кислотой — диазотирование, приводящая к диазосоединениям, широко применяемым в производстве красителей. А. с. чрезвычайно многочисленны и имеют большое практическое значение. Так, ароматич. нитросоединения, сульфокислоты, фенолы, амины являются полупродуктами синтеза многих красителей, лекарственных веществ; фенолы, стирол, терефталевую кислоту используют для синтеза полимеров; из толуола получают взрывчатое вещество тротил и т.д.
Характерные особенности этого класса соединений могут быть объяснены тем, что А. с. на самом деле не содержат чередующихся простых и кратных связей; все связи в бензоле равноценны и совершенно выравнены; расстояния между атомами углерода в бензоле ![]() промежуточны между значениями межатомных расстояний в случае простой
промежуточны между значениями межатомных расстояний в случае простой ![]() двойной
двойной ![]() связей. Поэтому строение бензола теперь предпочитают изображать не обычной формулой (1), а формулой (1а). Для бензола и др. А. с. характерно, что все p-электроны образуют устойчивую «замкнутую» электронную оболочку.
связей. Поэтому строение бензола теперь предпочитают изображать не обычной формулой (1), а формулой (1а). Для бензола и др. А. с. характерно, что все p-электроны образуют устойчивую «замкнутую» электронную оболочку.
Позже было найдено, что сходными с А. с. свойствами обладают и многие другие «небензоидные» соединения. В первую очередь следует назвать ненасыщенные пятичленные гетероциклические соединения типа фурана, тиофена, пиррола. Ароматическими свойствами обладают и шестичленные гетероциклические соединения типа пиридина.
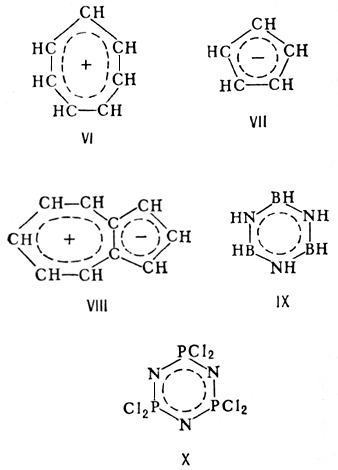
Известны небензоидные А. с., скелет которых состоит только из атомов углерода; к их числу относятся такие стабильные органические ионы, как катион тропилия (VI), анион циклопентадиенила (VII), биполярные соединения типа азуленов
(VIII) и др. Ароматическими свойствами обладают и некоторые неорганические соединения, например боразол (IX), фосфонитрилхлорид (X). Ароматичность бензоидных и небензоидных соединений, проявляющаяся в способности вступать в реакции электрофильного замещения, соответствует ряду: анион VII > пиррол > бензол ® пиридин > тропилий; способность к реакциям нуклеофильного замещения изменяется в обратном порядке.
Лит.: Карер П., Курс органической химии, пер. с нем., Л., 1960.
Я. Ф. Комиссаров.
- Эта статья или раздел использует текст Большой советской энциклопедии.